PD-L1 22C3 pharmDx「ダコ」の概要

非小細胞肺癌患者においてキイトルーダ® (ペムブロリズマブ)の適切な投与を行うための補助として用いるコンパニオン診断薬として承認されました。
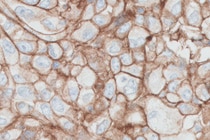
切除不能な進行・再発(未治療および既治療) の非小細胞肺癌患者においてキイトルーダ®の適切な投与を行うための補助として用いるコンパニオン診断薬として承認されました。
主な特長の詳細
PD-L1 IHC 22C3 pharmDx「ダコ」を肺癌パネルに加え、非小細胞肺癌患者への新たな治療オプションを提示可能にします。
検査の導入の詳細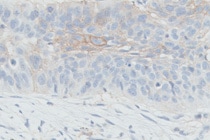
PD-L1 IHC 22C3 pharmDx「ダコ」のスコアリングガイドラインは、キイトルーダ®治療を行う患者の選定の際、PD-L1 発現率の確認に使用してください。
スコアリングガイドライン
キイトルーダ®の適切な投与を行うために必要な PD-L1 発現率の正確な測定およびスコアリングを習得するためのトレーニングです。
プログラムの詳細
非小細胞肺癌患者におけるキイトルーダ®の適切な投与を行うための補助を目的としたコンパニオン診断薬として承認されました。
- ダコ Autostainer Link 48 用に最適化された試薬
- 精度管理に適したコントロールスライドを含むキット構成
製品: PD-L1 IHC 22C3 pharmDx「ダコ」
専用染色装置: ダコ Autostainer Link 48
コード: SK00621-5J
1.PD-L1 IHC 22C3 pharmDx「ダコ」 - 添付文書
2.キイトルーダ®は、Merck & Co., Inc. の子会社である Merck Sharp & Dohme Corp. の登録商標です。治療にあたっては、キイトルー ダ®の添付文書をご参照ください。
3.Herbst RS, Baas P, Kim DW, Felip E, Pérez-Gracia JL, Han JY et al.Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial.Lancet 2016;387(10027):1540-50.
4.Reck M, Rodríguez-Abreu D, Robinson AG, Hui R, Csőszi T, Fülöp A et al.Pembrolizumab versus chemotherapy for PD-L1-positive non-small-cell lung cancer.NEJM 2016.DOI:10.1056/NEJMoa1606774.
体外診断用
PD-L1 IHC 22C3 pharmDx「ダコ」は、抗 PD-L1 マウスモノクローナル抗体(Clone 22C3)を用いた免疫組織化学染色法を原理としたアッセイキットあり、ダコ Autostainer Link 48 (IHC 自動染色装置)を用いて、ホルマリン固定パラフィン包埋(FFPE)非小細胞肺癌組織中の PD-L1 発現率を測定するためのものです。PD-L1 発現率は、任意の強度で部分的または完全な細胞膜の染色を示す陽性腫瘍細胞の割合である Tumor Proportion Score (TPS)を用いて決定します。
PD-L1 IHC 22C3 pharmDx「ダコ」は、PD-L1 低発現 (TPS ≧ 1%) である既治療の非小細胞肺癌患者において、キイトルーダ® ( ペムブロリズマブ) の適切な投与を行うための補助として用いることを目的としています。
PD-L1 IHC 22C3 pharmDx「 ダコ」 は、PD-L1 高発現 (TPS ≧ 50%) である未治療の非小細胞肺癌患者において、キイトルーダ® ( ペムブロリズマブ) の適切な投与を行うための補助として用いることを目的としています。
治療にあたっては、キイトルーダ®の添付文書をご参照ください。
体外診断用医薬品
承認番号 : 22800EZX00078000