手性化合物分离方法:液相色谱法,毛细管电泳法和二维液相法等

在做分析测试时经常听到手性化合物分析这个词,有些朋友已经非常熟悉了,但也有分析小白对此还比较懵懂。手性化合物指的就是分子量和分子结构相同但左右排列相反的两种化合物,就像我们的左右手一样。手性化合物虽然相似,但有时排列结构上的细微差异会造成手性化合物具有完全相反的性质,手性化合物分离是色谱分析中的重要问题之一。
多肽和蛋白的立体化学是合成多肽、非核糖体肽等产品结构表征和质量控制的重点和难点。近年来,随着合成多肽市场的稳步发展,质量控制的要求越来越高。除了准确分子量和氨基酸序列等常规的质量属性外,序列中无外消旋氨基酸杂质也是确保结构一致的重要因素。治疗型多肽中加入D-氨基酸是提高水解稳定性、改善药代动力学的重要手段之一;非核糖体肽是国内外新药创制的重要来源,其结构中常含有 D-氨基酸。同时,生物体中蛋白质氨基酸的外消旋化可影响其空间结构和功能,并证实与一些疾病的发生相关。氨基酸的手性分离检测如此重要,那让我们以手性氨基酸为例,一起来看看有哪些手性分离方法吧!
方法一:与手性衍生试剂反应生成非对映异构体——反相分离法
D-, L-型氨基酸与邻苯二甲醛(OPA),N-异丁酰-L-半胱氨酸,使用自动进样器自动衍生反应,生成非对映异构体,使用 Poroshell HPH-C18 色谱分离。
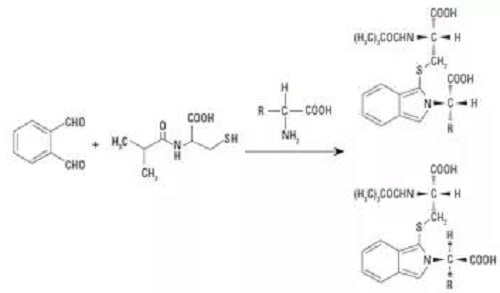
图为氨基酸与邻苯二甲醛(OPA),N-异丁酰-L-半胱氨酸衍生反应
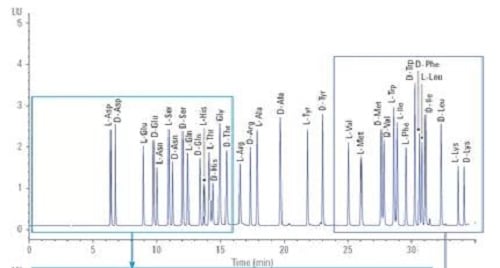
图为标样衍生分离色谱图
方法二: 手性填料——液相色谱/超临界流体色谱法
手性分离填料是通过化学涂覆或者键合方式将手性分离介质固定于硅胶或其他聚合物填料基质表面,通过手性固定相与手性分子间的相互作用,从而达到手性分离的目的。安捷伦 Poroshell 120 手性分离柱有四类手性分离介质可供选择:衍生化环果聚糖(Chiral-CF),羟丙基化 β-环糊精(Chiral-CD),以及大环内酯类抗生素的万古霉素(Chiral-V)和替考拉宁(Chiral-T)。
对于氨基酸的手性分析,推荐的首选色谱柱是 Poroshell Chiral-T。
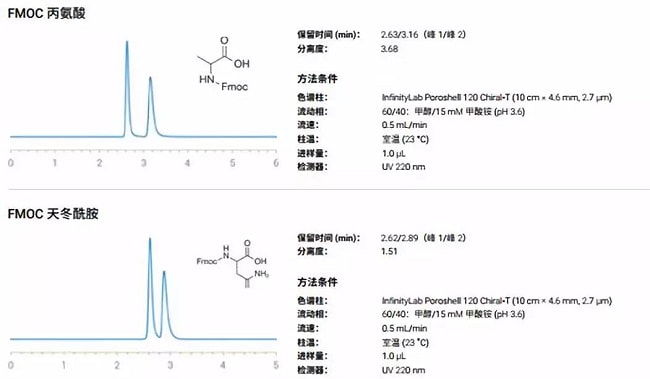
图为 Poroshell 120 Chiral-T 色谱柱反相条件对氨基酸 FMOC 衍生物的分离
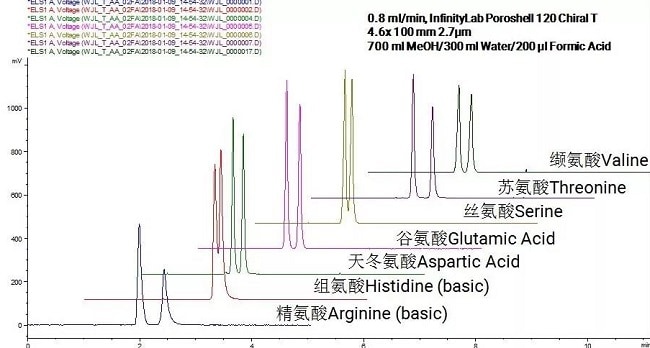
图为 Poroshell 120 Chiral-T 色谱柱反相条件非衍生的氨基酸
SFC 作为正相色谱的替代方法,常被用于手性化合物的分离。由于使用超临界流体作为流动相,其扩散系数和黏度接近于气体,因此溶质的传质阻力小,用作流动相可以获得快速高效分离;另一方面,超临界流体的密度与液体类似,具有较高的溶解能力,这样就便于在较低温度下分离难挥发、热不稳定性和相对分子质量大的物质。
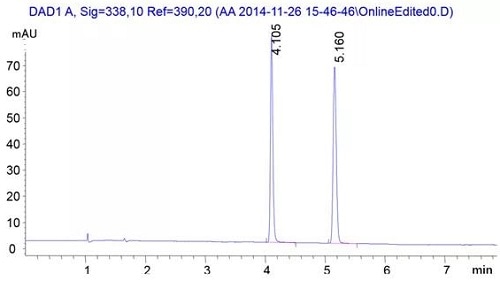
图为 SFC 分离 D/L-丙氨酰胺 OPA 衍生产物色谱图
方法三:毛细管电泳法(CE)
毛细管区带电泳是分离手性带电化合物的常用方法,环糊精是该方法中常用的手性选择剂。环糊精常由六个(α)、七个(β)、八个(γ)D-吡喃葡糖糖单元组成,腔体相对疏水而外表面亲水,其手性选择与其独特的结构和其本身的碳手性中心有关。
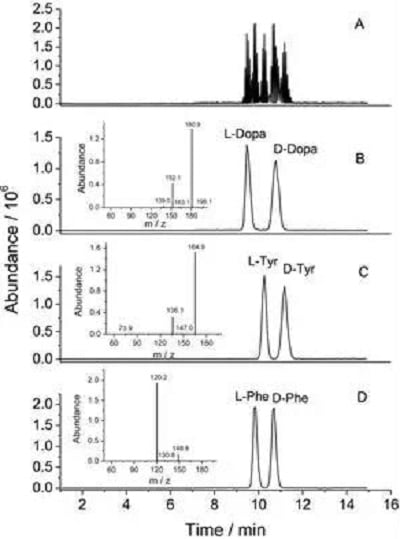
图为毛细管电泳分离 L-/D-DOPA, L-/D-Phe 和 L-/D-Tyr
方法四:二维液相色谱法(2D-LC)
全二维液相色谱用于分析 D 型和 L 型氨基酸 FMOC 衍生物,第一维色谱使用叔丁基氨基甲酰基奎宁手性固定相,第二维色谱使用叔丁基氨基甲酰基奎尼丁手性固定相。两种手性固定相对手性中心的选择性相反,从而使对映体在一维和二维的洗脱顺序刚好相反。非手性组分和杂质的峰在 2D 分离空间的对角线上排列,对映异构体在二维色谱图上交叉排列。此技术可以通过二维色谱图直接成像氨基酸的构型。全二维液相成像生动直观的展示了氨基酸手性异构体的分离结果,适用于多肽药物发现、杂质分析和天然产物的分析。
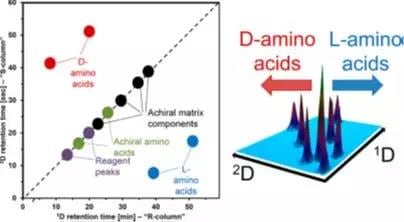
图为手性-手性二维成像分离示意图
