Access Agilent 电子期刊,2013 年 9 月
>> 更新资料 | 订阅 Access Agilent | 文章目录
准确肽谱分析的指南
作者:James Martosella
安捷伦生物制药应用科学家,CSD 生物应用部
肽谱是一个蛋白及其多次处理后所得最终产物的指纹图谱,可为所分析的蛋白提供一个全面深入的认识。它包括四个主要步骤:蛋白质分离和纯化、肽键的选择性裂解、肽段的色谱分离以及肽段的验证分析。
肽谱是一个比较流程,它可以确定蛋白的一级结构,并检测结构的改变。此外,它可证实工艺一致性和遗传稳定性。肽谱中应包含足够多的肽段以提供有意义的信息,包括蛋白质的阳性鉴定、完整肽段序列的最大覆盖率,并提供非消解蛋白水平所得信息之外的其他信息和测序鉴定。
因为一张谱图可能包含 100 多个色谱峰,代表不同的肽段及其衍生物,所以需要分析人员具备样品前处理方法、强大分离技术和验证方案方面的知识。
蛋白质降解改善肽谱分离
虽然蛋白质酶解过程的优化有许多选择,但仍涉及一些常见步骤(表 1)。
步骤 |
预期效果 |
常规实验 |
|---|---|---|
1. 样品前处理 |
准备样品用于降解 |
去除、富集、透析、脱盐 |
2. 选择降解试剂 |
特异性降解要求 |
化学或酶降解。常用胰蛋白酶,因为其具有良好的特异性。 |
3. 还原和烷基化 |
还原 — 还原硫键 |
还原 — DTT,45 分钟,60 °C |
4. 降解过程 |
蛋白质降解 |
降解 — pH 8,37 °C,过夜 |
5. 富集/纯化 |
前处理用于 LC 或 LC/MS 的样品 |
C18 枪头、浓缩、透析、亲和色谱柱 |
表 1. 蛋白质降解的五个步骤
成功肽谱分析的关键因素
最常用的肽谱分析色谱柱方法(特别是在生物制药领域)是反相色谱法 (RPC)。一般情况,在开发实用性 RPC 肽谱分析方法时需要很好地了解肽特异性色谱柱的选择要求以及色谱方法开发过程。虽然很多相同的色谱原理同时适用于多肽和小分子分离,但在优化多肽方法中,还是有许多条件特异性变量(表 2)。
变量 |
特性 |
优势 |
|---|---|---|
色谱柱 |
表面多孔 |
扩散路径更短,可在较高的线性速度下分离较大的分子,不会出现系统反压增加的问题,并获得更好的峰形和分离度 |
流动相 |
添加剂,例如 TFA、甲酸、乙酸 |
通过与多肽的带电基团形成离子对而提高多肽的疏水性 |
检测 |
280 nm,同时使用 210 nm |
色氨酸、酪氨酸及苯丙氨酸在 280 nm 下非常灵敏,而 210 nm 检测对许多其他的生物制剂而言相对选择性较差 |
表 2. 多肽方法优化变量
开发高效的肽谱分析方法
肽谱分析结果会基于方案的不同而有所差异。考虑以下五个步骤中的因素将帮助您确定满足您独特的谱图分析要求的最有效方法:
第一步:选择初始梯度条件下的柱长、流动相组成、流速、温度及检测器。应针对保留性 (k’) 优化初始分离,这要求梯度的陡度不能太大
第二步:调整梯度范围,通过减少色谱图开始和结束处浪费的空间,最大程度缩短运行时间。
第三步:改变选择性;如果观察到重叠的谱带或运行时间过长,可以尝试调整选择性。
第四步:梯度形状;通过使用非线性梯度形状作为进一步改善分离的方法,实现更宽的谱带间隔。
第五步:改变色谱柱条件;在优化了谱带间隔和选择性后,需考虑改变运行时间和柱长以改善分离度和分析速度。
利用质谱进行肽谱表征
RPC 结合质谱 (MS) 是表征多肽和肽谱(表 3 )的理想方法。
肽谱分析应用 |
质谱类型 |
优势 |
|---|---|---|
确认特定蛋白质的种类 对蛋白质进行详细表征(例如确认 N 端和 C 端多肽、高序列覆盖率肽谱、氨基酸取代等) 筛查和鉴定翻译后修饰(例如糖基化、二硫键、N 端焦谷氨酸、甲硫氨酸和色氨酸氧化等) |
电喷雾、MALDI-TOF-MS 以及快速原子轰击 (FAB) |
通过将蛋白水解多肽完整电离为气相测量精确质量 |
串联质谱 |
对修饰后蛋白进行测序,并确定氨基酸修饰类型 |
|
四极杆飞行时间 (QTOF) |
因具有高分辨率和质量准确性,可提供更多的结构信息,特别是对于较大的多肽 |
 放大图片
放大图片
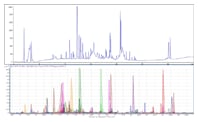
图 1. 优化的 EPO 蛋白质肽谱,序列覆盖率 100%。顶部色谱图展示了使用 2.1 x 150 mm AdvanceBio 肽谱分析色谱柱对完全优化的 EPO 消解物进行分析所得到的肽谱分离图。底部色谱图展示了针对 Agilent Q-TOF 生成的序列覆盖率所进行的定性分析(使用分子特征提取器)
表 3. 利用质谱进行肽谱分析
图 1 展示了经过高度优化后,所得的红细胞生成素蛋白质 (EPO) 降解物的 ESI-MS 肽谱。优化色谱条件和质谱参数后,可获得 100% 的序列覆盖率。
了解肽谱分析过程和选项的更多信息
肽谱分析(生物制药行业的重要工具)是一款非常强大的方法,广泛用于蛋白质的鉴定测试,尤其适用于重组方式生成的蛋白。浏览全新的安捷伦出版物《最优化肽段表征的关键条件:肽谱分析指南》,了解更多信息。
>> 更新资料 | 订阅 Access Agilent | 文章目录
