PD-L1 IHC 28-8 pharmDx for Gastric Cancer


CheckMate -649 試験は、未治療の HER-2 陰性の進行または転移性胃がん(胃食道接合部癌を含む)患者を対象とした多施設無作為化非盲検第 Ⅲ 相臨床試験です。
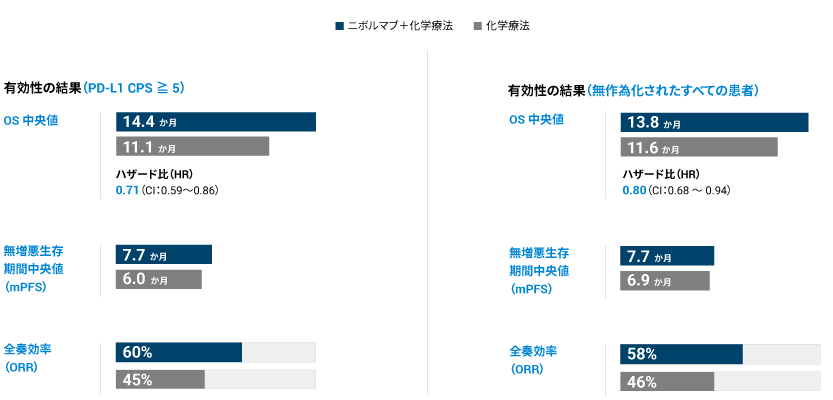
CheckMate -649 試験の結果により、ニボルマブと化学療法(フッ化ピリミジン系抗悪性腫瘍剤及びプラチナ製剤)の併用療法の有効性の程度は、PD-L1 発現(CPS)の値に関連する事が示されました。
CHECKMATE-649 試験でのすべての患者における PD-L1 発現の割合は 82 % でした。また、PD-L1 発現が CPS 5 以上の患者の割合は 60 % でした。
PD-L1 IHC 28-8 pharmDx「ダコ」は、体外診断用医薬品として厚生労働省により承認されています。また感度、特異性、正確性など検査に必要な性能条件を備えていることが実証されています。
| 検証パラメータの例 | 仕様 |
|---|---|
| 特異性 |
|
| 感度 |
|
| 同一施設内での再現性 |
|
| 複数施設間での再現性 |
|
OA = 全体一致率
| 製品 | 型番 |
|---|---|
| PD-L1 IHC 28-8 pharmDx「ダコ」 | SK00521-5J |
|
キットとは別にご用意いただく必要のあるもの: ダコ Autostainer Link 48(IHC 自動染色装置) ダコ EnVision FLEX 洗浄液(20 x) ダコ EnVision FLEX ヘマトキシリン(AutostainerLink 用) PT Link PT Link リンスステーション |
AS48030 K800721-2 K800821-2 PT101/PT200 PT109 |
- CHECKMATE-649 試験
- PD-L1 IHC 28-8 pharmDx「ダコ」添付文書
- ニボルマブ添付文書:小野薬品工業株式会社/ブリストル・マイヤーズ スクイブ株式会社
使用目的
体外診断用医薬品
がん組織、細胞中の PD-L1 発現率の測定
- ニボルマブ(遺伝子組換え)の非小細胞肺癌患者、頭頸部癌患者又は胃癌患者への適切な投与を行うための補助に用いる。
- ニボルマブ(遺伝子組換え)及びイピリムマブの併用療法の悪性黒色腫患者への適切な投与を行うための補助に用いる。
PD-L1 IHC 28-8 pharmDx「ダコ」で PD-L1 発現率を測定し、以下の医薬品の投与可否を判断することが望ましい。
- 化学療法既治療の非扁平上皮非小細胞肺癌患者及び頭頸部癌患者におけるニボルマブ(遺伝子組換え)
- 化学療法未治療の非小細胞肺癌患者及び胃癌患者におけるニボルマブ(遺伝子組換え)と化学療法の併用療法
- 悪性黒色腫におけるニボルマブ(遺伝子組換え)とイピリムマブの併用療法
ただし、PD-L1 IHC 28-8 pharmDx「ダコ」を用いて PD-L1 発現率を測定することができない場合には、ニボルマブ(遺伝子組換え)及びイピリムマブの添付文書等を参照の上、投与の可否を適切に判断すること。
PD-L1 検査の指針となる特定の臨床状況については、ニボルマブの添付文書をご参照ください




